Телеграм-боты стали неотъемлемой частью бизнес-стратегий и ежедневной коммуникации благодаря своей функциональности и удобству использования.
Обеспечение качественного и сбалансированного питания для строителей на удаленных объектах является одним из важных
В статье рассмотрим принцип работы водяных теплых полов, их преимущества, а также критерии выбора
Процесс элитного ремонта начинается с тщательного планирования и разработки дизайн-проекта, который учитывает все пожелания
Использование готовых строительных смесей имеет ряд неоспоримых преимуществ перед традиционными методами приготовления растворов.
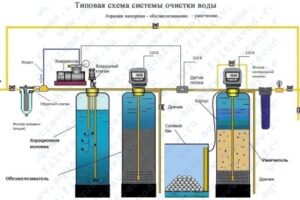
Системы обезжелезивания играют ключевую роль в обеспечении качества воды в различных секторах, от бытового
Внедрение прецизионной лазерной резки в производственный процесс открывает новые перспективы для компаний, стремящихся к
Приём лома алюминия играет критическую роль в индустрии переработки металлов, поскольку алюминий является одним
Освещение в медицинских учреждениях играет критически важную роль в обеспечении качества и безопасности медицинского
Использование клинового анкера позволяет обеспечить надежное и долговременное крепление, что критически важно для безопасности
Термопанели с клинкерной плиткой представляют собой инновационное решение для облицовки фасадов зданий, которое сочетает
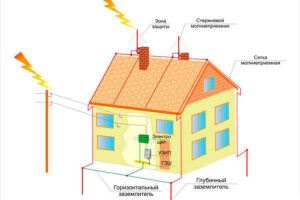
В данной статье мы подробно рассмотрим, как устроены молниеотводы, как они работают и каковы
В этой статье мы рассмотрим, почему важно проводить обеспыливание стяжки и какие методы и
Сауна — это не только место для релаксации и восстановления сил, но и значимый
Котельное оборудование является сердцем любой системы отопления, обеспечивая тепло для жилых домов, коммерческих и
Стеллажи играют ключевую роль в организации складских помещений, обеспечивая оптимальное использование пространства и удобство
Шарикоподшипники — это тип подшипников качения, в котором используются шарики в качестве катущего элемента.
Бордюр для тротуарной плитки не только выполняет декоративную функцию, но и играет важную роль
Выбор подходящего манипулятора - это ключевой момент, который определяет эффективность и безопасность проведения грузоподъемных
Проектирование начинается с анализа состава сточных вод и оценки их количества, что позволяет определить
Тайланд - страна, которая не перестает привлекать внимание инвесторов и любителей тропического климата своим
Светодиодные трубки стали символом новой эры в области освещения, объединяя энергоэффективность, долговечность и высокое
Рынок недвижимости в Уфе продолжает развиваться, приспосабливаясь к изменяющимся требованиям жителей и экономическим условиям.
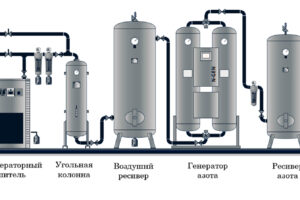
Генераторы азота и кислорода представляют собой передовые технологические решения, предназначенные для производства азота и
Для обеспечения эффективной работы дренажной системы, необходимо тщательно подходить к выбору типа дренажных труб.
Модульные блочные котельные (БМК) представляют собой инновационное решение в области систем отопления и горячего
Выбор надежной компании для аренды автомобиля является ключевым фактором, гарантирующим качественный сервис и комфортную
Регистрация торговой марки является важным шагом для любого бизнеса, стремящегося защитить своё название, логотип
Дорожная сетка – это ключевой элемент в строительстве и ремонте дорожного покрытия, играющий важную
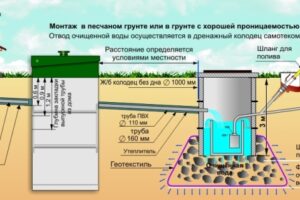
Монтаж автономной канализации – это важный этап обустройства загородного дома или коттеджа, который требует